
特聘研究员
免疫学,分子生物学,病毒学
guoxunwang(at)szbl.ac.cn
2025 至今 深圳湾实验室 传染病研究所 特聘研究员
2017-2024 美国西南医学研究中心 博士后、讲师
2012-2016 中国科学院 博士
实验室将聚焦肠道病毒的病原学和宿主抗病毒免疫反应,探寻肠道病毒如何与宿主细胞表面的特异受体结合以及病毒感染引起的细胞死亡的机制研究,通过对肠道病毒生活史和宿主抗病毒免疫反应的研究为研发抗病毒药物以及疫苗提供理论支撑。目前课题组主要研究方向包括:(1)肠道病毒受体的鉴定及对其功能的研究;(2)肠道病毒释放与其感染引起的细胞死亡机制的研究;(3)肠道病毒疫苗的研发。
王国勋博士围绕宿主与病原微生物互作的核心枢纽-细胞死亡进行了深入的研究,迄今为止以第一作者身份在Nature,Cell Host Microbe,Journal ofVirology等杂志,并以共同作者身份在Science,Science Immunology,Nature Nanotechnology,Science Advance等杂志发表研究论文。主要研究成果包括:发现了一种新的由病毒感染诱导的宿主细胞死亡方式,并揭示了在与宿主的长期共演化过程中,病毒通过获取宿主执行细胞死亡功能蛋白的破膜结构域来主动起始感染细胞的死亡,进而帮助其在宿主组织中扩散的新机制(Nature, 2023)。该研究拓展了对细胞死亡尤其是病毒感染引起的细胞死亡的新的认识,也提供了一个新的潜在的抗病毒治疗靶点;通过对植物和病原细菌的研究,鉴定了植物胞内免疫受体蛋白识别细菌毒性蛋白并激活免疫反应,进而引起细胞死亡的完整信号通路(Cell Host Microbe, 2015),并借助该免疫识别系统参与发现并解析了植物的抗病小体。此研究不仅回答了植物抗病领域重要的科学问题即胞内免疫受体蛋白如何被激活并介导免疫反应,同时也为培育和改良抗病作物提供了坚实的理论基础。
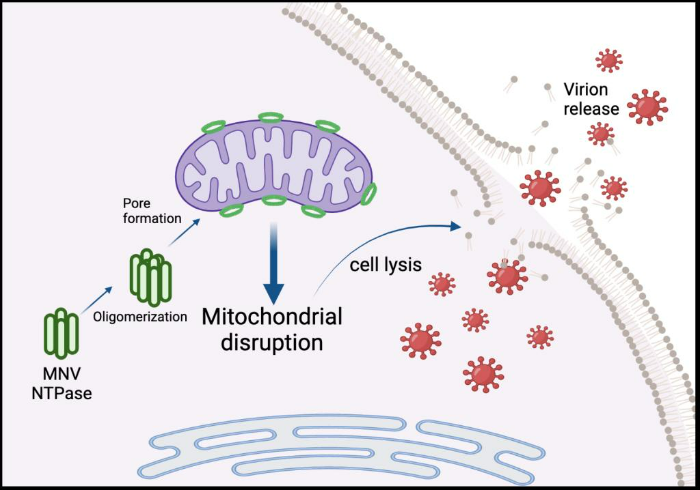
诺如病毒通过编码破膜蛋白主动起始细胞死亡进而完成病毒的释放
2015年 博士生国家奖学金
2015年 遗传发育所益海嘉里优秀博士生奖
1. Wang GX, Zhang D, Orchard RC, Hancks DC, Reese T. Norovirus MLKL-like protein initiates cell death to induce viral egress.Nature, 2023. 616:152-158.
2. Wang GX, Zarek C, Chang T, Tao LL, Lowe A, Reese T. Th2 cytokine modulates herpesvirus reactivation in a cell type-specific manner.Journal of Virology,2021.95: 8.
3. Wang GX, Roux B, Feng F, Guy E, Li L, Li N, Zhang X, Lautier M, Jardinaud MF, Chabannes M, Arlat M, Chen S, He C, Noël LD, Zhou JM. The decoy substrate of a pathogen effector and a pseudokinase specify pathogen-induced modified-self recognition and immunity in plants.Cell Host Microbe,2015. 18: 1-11.
4. Wang JZ, Hu MJ, Wang J, Qi JF, Han ZF, Wang GX, Qi YJ, Wang HW, Zhou JM, Chai JJ. Reconstitution and structure of a plant NLR resistosome conferring immunity.Science, 2019. 04, 364 (6425).
5. Wang JZ, Wang J, Hu MJ, Wu S, Qi JF, Wang GX, Han ZF, Qi YJ, Gao N, Wang HW, Zhou JM, Chai JJ. Ligand-triggered allosteric ADP release primes a plant NLR complex.Science, 2019. 04, 364 (6435).
6. Zhang D, Wang GX, Yu X, Wei T, Farbiak L, Johnson LT, Taylor AM, Xu J, Hong Y, Zhu H, Siegwart DJ. Enhancing CRISPR/Cas gene editingthrough modulating cellular mechanical properties for cancer therapy.Nature Nanotechnology,2022. 05, 17(7): 777-787.