冷冻电镜领域的“分辨率革命”(resolution revolution)在过去12年间改变了结构生物学的格局,许多之前难以解析的生物大分子及其复合物的高分辨率结构纷纷被报道。然而,以解析已知大分子结构为目的的传统生物学还远远没有发掘出冷冻电镜的潜力。过去三年,颜宁团队在探讨这样一个问题:
作为当前分辨率最高的显微技术,我们还可以用冷冻电镜做什么?我们是否可以把冷冻电镜作为发现工具,去探索深地、深海、深空,发现新的物种和物质?
为此,颜宁团队开始了一个新的把高分辨率三维结构作为发现起点的研究范式(a structure-first paradigm): 酷寻(CryoSeek)。作为概念验证,在探索深海等领域之前,团队先探索了清华著名的荷塘,竟然意外解析了大量糖质的结构,弥补了结构生物学在糖质领域研究的巨大空白,因此将之命名为“荷糖月色”计划。
糖质(Glycan)是四大基本有机生物大分子之一,同时也是地球上含量最高的生物有机分子(biomass)。它们不仅是重要的能量来源和细胞结构组成成分,还广泛参与多种关键生命过程,如蛋白质折叠、细胞识别及免疫反应等。然而,与核酸和蛋白质相比,糖类的结构生物学研究明显滞后。这主要源于糖类在单糖组成、分支模式、空间构型及结构柔性等方面的高度复杂性,使其三维结构解析面临巨大挑战。因此,糖质常被称为生命科学领域的“暗物质”。而高分辨率结构信息的缺乏,不仅限制了我们对糖质功能及其作用机制的深入理解,也制约了基于人工智能的结构预测与设计的发展。
在前期研究中,颜宁团队结合冷冻电镜分析、AI辅助的自动建模以及生物信息学分析,报道了来自清华大学荷塘环境样品的一种纤维蛋白结构TLP-1,并对其来源和潜在功能进行了推测。随后的研究进一步鉴定出一种新型糖纤维结构TLP-4,其核心是由四肽重复序列组成的线性多肽,外围被厚厚的糖链包裹。四肽重复片段包含一个保守的3,4-二羟脯氨酸 (3,4-dihydroxyproline, DiHyp) ,其3-OH与4-OH均被糖基化修饰。与DiHyp相邻的位置,还存在一个保守的O-糖基化修饰的丝氨酸或苏氨酸。这些研究成果,不仅揭示了聚糖在生物大分子结构组装过程中的重要作用,也表明以结构为先的CryoSeek研究策略为天然糖质等生命“暗物质”的发现与结构解析提供了新的研究范式 [1,2]。
北京时间2026年4月20日,颜宁团队及其合作者在《细胞-化学生物学》(Cell Chemical Biology)杂志发表了题为“通过酷寻鉴定具有多样化学组成和结构组装形式的糖纤维结构”(CryoSeek identification of glycofibrils with diverse compositions and structural assemblies) 的最新研究成果(图1)。延续“荷糖月色”研究计划,研究团队进一步报道了六种全新的糖纤维结构,揭示了糖纤维结构在天然环境中的多样性以及在结构组装过程中的关键作用。

图1. 文章首页
新解析的六种糖纤维结构分别被命名为TLP-IPT、TLP-12、TLP-4b、TLP-3、TLP-2和TLP-0(图2)。其中名称前缀的TLP源自清华大学荷塘(Tsinghua Lotus Pond),后缀则反映了各糖纤维中蛋白核心的结构特征。TLP-IPT是由连续的IPT(Ig like/plexins/transcription factors)结构域构成可识别的蛋白核心,每个IPT结构域外围连接着13条糖链,且整体结构从切面观察呈现“C”字型构象;而邻近的IPT结构域上连接的糖链,能够将“C”字型结构进行补齐,从而形成完整的“O”型环状结构。TLP-12是由三股高度重复的十二肽共同编织成三股平行β折叠带,其外围覆盖两列呈螺旋排列的糖链,整体呈现螺旋状结构。
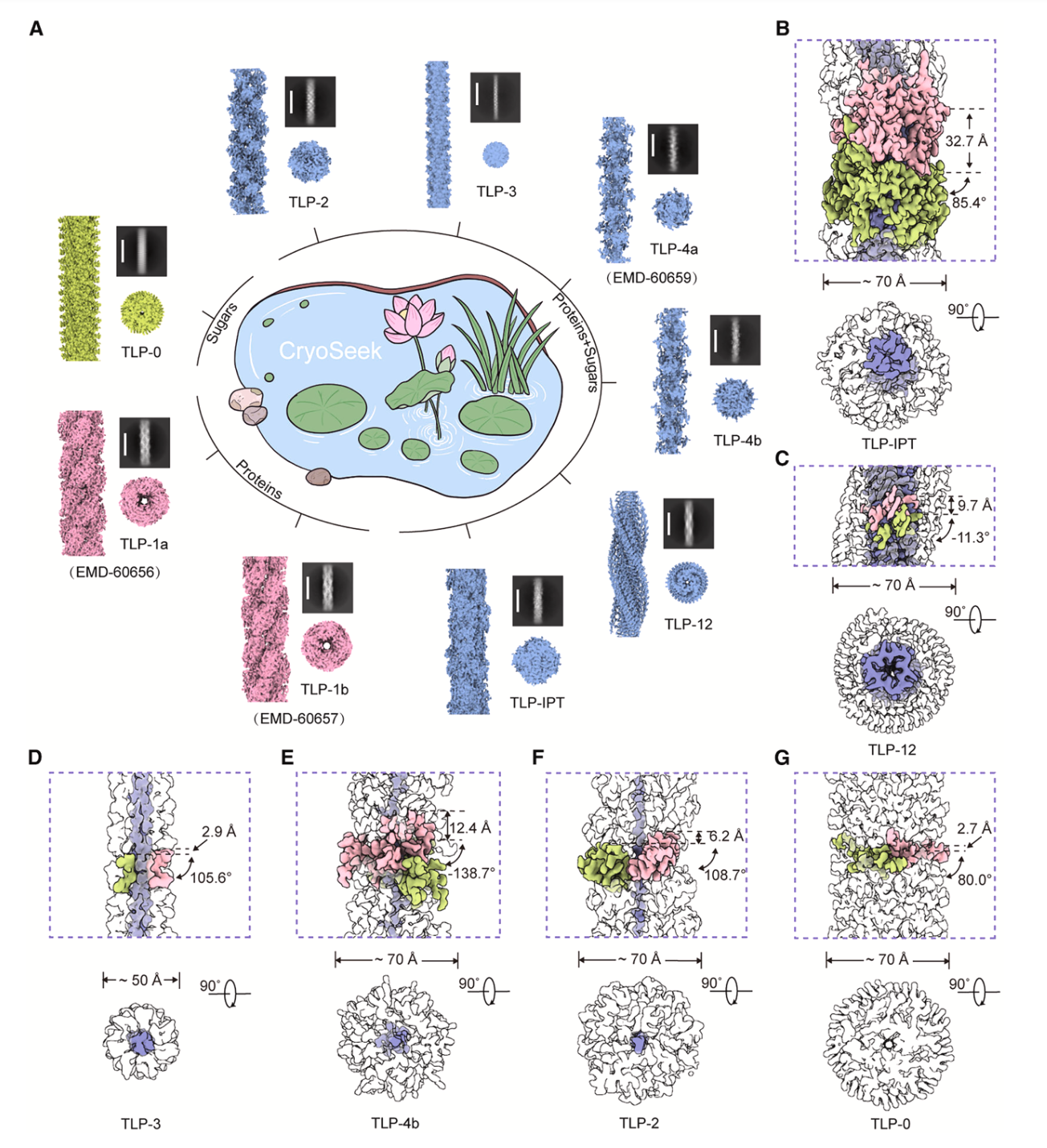
图2. 利用CryoSeek研究策略,在清华荷塘中鉴定出多种纤维结构。(A)目前,在清华荷塘水样中共解析出9种高分辨率纤维结构,依据其蛋白组成可分为三种类型,分别为蛋白纤维(TLP-1a/b)、以蛋白为核心的糖纤维(TLP-2/3/4a/4b/12/IPT)和全部由糖组成的纤维(TLP-0);(B-F)最新报道的5种糖纤维结构的组成以及其螺旋参数。
TLP-4b、TLP-3和TLP-2的共同特征是其核心均为线性多肽,外层由糖链包裹。其中,TLP-3由三股三肽重复序列互相缠绕,形成蛋白细芯;而TLP-4b和TLP-2的核心则是由一条线性多肽组成。TLP-4b的核心是四肽重复序列,在分子组成上与之前解析的TLP-4类似,均包含一个保守的3,4-二羟脯氨酸,一个可以被O-糖基化修饰的丝氨酸或苏氨酸,以及另外两个非保守的氨基酸组成。尽管两者的蛋白核心相似,其外圈连接的糖链组成与分支形式存在明显差异,因此研究团队将之前解析的TLP-4重新命名为TLP-4a,并将新解析的命名为TLP-4b。与之相对应的,TLP-2的核心则为二肽重复序列,基于冷冻电镜密度,研究团队推测其糖基化修饰形式可能为磷酸糖基化修饰(Phosphoglycosylation)。
尤为引人注目的是TLP-0的结构,其完全由糖类组成,其中“0”表示不含有蛋白组分。TLP-0的核心是由三糖重复单元以螺旋的形式排列,每个重复单元上连接有约18个额外的糖分子,这些糖链对整体结构的稳定与组装至关重要。同时,TLP-0在分子组成及组装方式上均显著不同于纤维素、淀粉和糖原等经典聚糖,揭示了糖类结构的高度多样性,并表明聚糖可在不依赖蛋白的情况下自发组装形成具有高级有序结构的超分子体系(图3)。
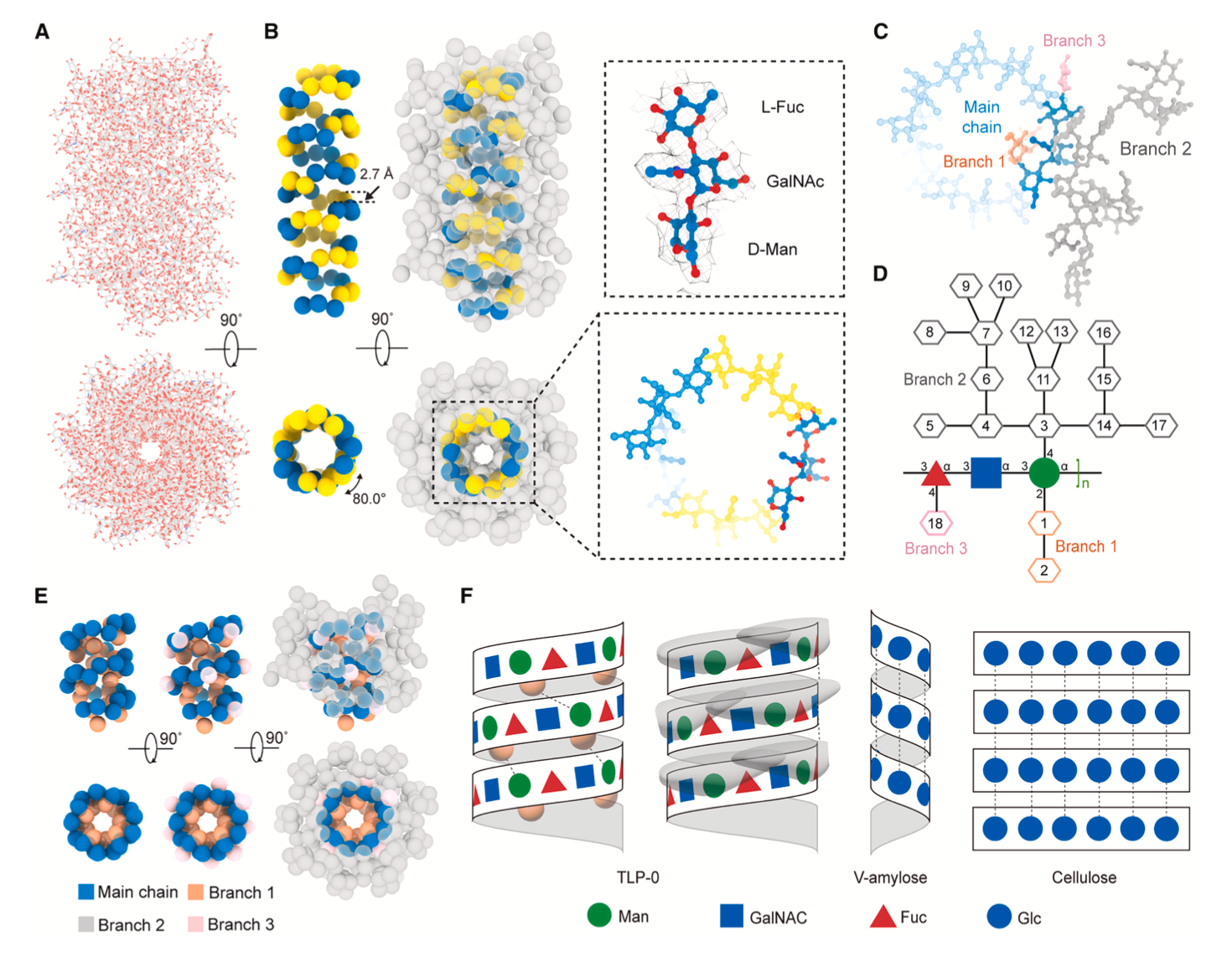
图3. TLP-0的分子组成与组装形式
上述研究揭示了天然环境中糖纤维的多样性,表明在CryoSeek这一“结构先行”的生物学发现新范式下,结合多学科研究手段,有望为糖质等生命“暗物质”的发现、高通量结构解析以及体系化研究提供全新路径。同时,以“荷糖月色”为抓手,CryoSeek策略已建立了标准化、高通量的研究流程,可以进一步拓展至深海、深地、深空等尚未充分探索的生物环境,从而推动对生命世界更深层次的认识与理解。
深圳医学科学院创始院长、深圳湾实验室主任颜宁,清华大学生命科学学院助理研究员李张强和2025年毕业的博士生王彤彤为本文的共同通讯作者。李张强、王彤彤以及2023级直博生孙熠彤为本文共同第一作者。清华大学生命科学学院博士后徐魁、博士后黄文泽、副教授张强锋、副教授闫创业,以及深圳医学科学院的胡名旭研究员,为本研究做出了重要贡献。实验的冷冻电镜数据收集得到了清华大学冷冻电镜平台的帮助,实验的计算工作得到清华大学高性能计算平台、国家蛋白质设施实验技术中心(北京)的支持。本研究得到了国家自然科学基金重大研究计划,北京生物结构前沿研究中心与清华-北大生命科学联合中心的经费支持。同时,特别感谢鹏瑞基金会捐赠的“迈瑞教授”席位,对颜宁研究工作给予的支持。
本研究中所报道解析的糖纤维结构及其对应的冷冻电镜密度图目前已上传至CryoSeek数据库(https://cryoseek.org.cn/)。CryoSeek数据库是由颜宁团队依托深圳医学科学院建立,系统收录了以糖质为代表的“生命暗物质”的结构与鉴定成果,并提供在线服务,从而更好地支持糖质等相关结构数据的管理与共享,服务于科研界。CryoSeek数据库以及高通量CryoSeek结构测定技术体系的相关研究成果已发布于浪淘沙预印本平台 [3]。
值得关注的是,这一最新论文引用了两篇此前发布于浪淘沙预印本平台上的研究手稿:
High-throughput cryo-EM characterization and automated model building of glycofibrils via CryoSeek
AI-facilitated high-resolution cryo-EM analyses of tubular mastigonemes reveal the structural roles of N- and O-glycans
这两篇预印本文章通过浪淘沙平台向全球公开,不仅为后续研究提供了重要参考,更印证了预印本在学术交流中的关键价值——在正式发表前,预印本同样可以被规范引用。目前,发布在浪淘沙预印本平台上的文章已逐步被Google Scholar、ResearchGate等主流学术平台收录,学术影响力持续扩大。

图4. 浪淘沙预印本文章被引用
参考文献:
[1] Wang, T., Li, Z., Xu, K., Huang, W., Huang, G., Zhang, Q. C., & Yan, N. (2024). CryoSeek: A strategy for bioentity discovery using cryoelectron microscopy. Proceedings of the National Academy of Sciences, 121(42), e2417046121.
[2] Wang, T., Huang, W., Xu, K., Sun, Y., Zhang, Q.C., Yan, C., Li, Z., & Yan, N. (2025). CryoSeek II: Cryo-EM analysis of glycofibrils from freshwater reveals well-structured glycans coating linear tetrapeptide repeats. Proceedings of the National Academy of Sciences, 122(1), p.e2423943122.
[3] Hu, M., Chen, S., Wang, T., Qin, L., Zhang, Q., Zhang, Y., Ge, Q., Chen, T., Li, M., Li, C., Xu, G., Gui, Q., Li, Z., & Yan, N. (2025). High-throughput cryo-EM characterization and automated model building of glycofibrils via CryoSeek. LangTaoSha Preprint Server. https://doi.org/10.65215/bkvrt910