睡眠与觉醒之间的转换,是机体最基本的状态切换之一。睡眠过程中,不仅大脑活动改变,也伴随着感知、行为和生理活动的一系列变化。例如,由清醒进入睡眠时,往往伴随着血压、心率、呼吸频率的下降。与此同时,外周生理状态的改变也能够显著影响睡眠-觉醒状态,并对机体稳态恢复至关重要。比如,感染发生时,机体常常表现出嗜睡,以促进恢复。那么,大脑状态与外周生理活动是如何协同调控的?
近日,深圳医学科学院(SMART)神经调控与认知研究所(Institute of Neuromodulation and Cognition, INC)丹扬团队和姚园园团队在Annual Review of Neuroscience在线发表题为 Body-Brain Integration: The Lower Brainstem in Sleep-Wake Regulation 的综述文章,系统总结了下位脑干在睡眠-觉醒调控中的最新研究进展,并提出:睡眠不仅是由中枢神经系统内部网络主导的大脑状态变化,也是机体应对外周稳态需求的一种主动输出;身体内部状态经脑干整合,最终全身性协同调控大脑状态与机体稳态。
数十年来,睡眠研究主要强调前脑和下丘脑在睡眠调控中的主导作用。然而,近年来的研究重新唤起了人们对下位脑干的关注。下位脑干长期以来被认为主要参与自主神经活动和躯体运动控制。然而,越来越多的研究表明,下位脑干并非被动的信息中继站,而是把身体内部状态与大脑状态调控联结起来的整合枢纽(图1),能够将来自心血管、呼吸、消化和免疫等系统的内感受信号转化为睡眠或觉醒驱动力,从而使大脑状态与机体稳态需求相匹配。

图1. 脑干是连接内脏生理与躯体运动、自主神经活动及睡眠-觉醒状态调控的关键枢纽。
孤束核(nucleus of the solitary tract, NST)接收来自心血管、呼吸和消化系统的内感受信号,同时也感知免疫等信号。传统上,孤束核被视为调节单个稳态系统的中枢,例如通过压力反射调控血压。越来越多的证据表明,孤束核也是一个重要的睡眠调控枢纽。它能够将血压波动、免疫激活等外周信号转化为睡眠驱动力(图2),从而帮助脑状态与机体内部状态相协调。换句话说,孤束核不仅是内脏感觉信息进入大脑的重要门户,也可能是将“身体状态”转化成“睡眠需求”的关键节点。
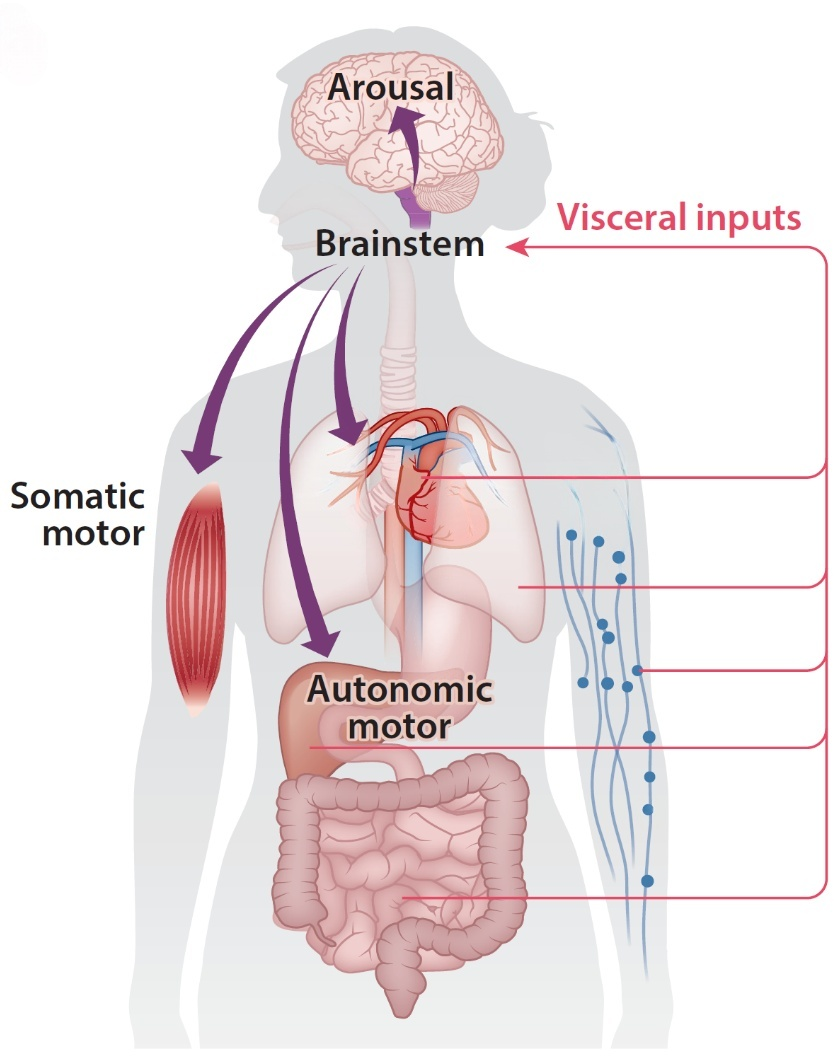
图2. 血压压力反射环路协同调控心血管活动和睡眠。
臂旁核(parabrachial nucleus, PBN)在处理威胁相关输入、促进觉醒方面具有关键作用。臂旁核是一个重要的危险信号检测中枢,整合内感受输入与痛觉等躯体感觉输入以及缺氧等化学感觉输入,从而协调生存相关行为,并在促进觉醒方面发挥关键作用。
值得注意的是,其中一部分臂旁核神经元也可能具有促睡眠作用,参与疾病相关睡眠、温暖环境诱导的睡眠等。未来研究可以进一步探索臂旁核的其他功能例如液体摄入调控等是否也与睡眠-觉醒调控存在相互作用。
睡眠并不只是“意识状态变了”,而往往伴随着一整套全身性变化,包括肌张力下降、行为活动抑制以及自主神经活动改变。延髓多个核团的GABA能神经元在这些变化的协调中发挥重要作用。腹内侧延髓(ventromedial medulla, VMM)GABA能神经元接受来自脑桥亚外侧背核的谷氨酸能输入,在REM睡眠期间呈现激活状态,介导REM睡眠期间的肌张力缺失;还可通过对蓝斑核、背缝核以及腹侧被盖区中单胺能神经元的抑制促进NREM睡眠;通过向脊髓发出的下行投射调节自主神经运动输出。尾腹外侧延髓(caudal ventrolateral medulla, CVLM)GABA能神经元是血压压力反射的主要抑制节点,通过抑制腹外侧延髓(rostral ventrolateral medulla, RVLM)中的儿茶酚胺能神经元,降低交感神经输出和血管张力,并增加NREM睡眠。面神经旁核(parafacial zone, PZ)GABA能神经元抑制臂旁核促进NREM睡眠。
尽管腹侧延髓多个亚区都能抑制运动活动,但它们对睡眠-觉醒状态的影响却各不相同:有的促进NREM睡眠,有的则促进REM睡眠。系统绘制这些区域的功能图谱,并鉴定决定某一特定神经元群体促进REM还是NREM睡眠的分子和连接特征将至关重要。
睡眠伴随与呼吸、心率等自主神经相关活动变化。近年来研究显示,疑核(ambiguus nucleus, AMB)胆碱能神经元,以及腹外侧延髓和蓝斑(locus coeruleus, LC)中的儿茶酚胺能神经元,这些与自主神经活动调控密切相关的神经元也参与睡眠-觉醒状态调节。
疑核胆碱能神经元通过投射至心脏、肺、食管、咽和喉,调控心血管、呼吸以及上消化道功能。令人意外的是,激活疑核胆碱能神经元不仅会降低动脉血压和心率,还会促进NREM睡眠,提示其可能参与协调心血管活动与大脑状态转换。
腹外侧延髓儿茶酚胺能神经元会在生理性应激条件下被激活,并协调自主神经、代谢和神经内分泌反应,以促进机体生存。研究表明,光遗传激活RVLM儿茶酚胺能神经元可迅速诱导觉醒。由于缺氧和低血压这两种代表潜在的生命威胁的刺激能够强烈激活这些神经元,因此这些神经元的促觉醒效应很可能有助于机体迅速产生对生存至关重要的行为反应。
蓝斑核去甲肾上腺素能(norepinephrinergic, NE)神经元整合环境、内脏和认知信息,并向全脑、脊髓广泛投射,参与行为状态、躯体和自主神经运动功能的调控。这些神经元将脑觉醒状态与自主神经和躯体运动控制连接起来,从而确保状态转换与外部挑战和机体内部生理需求相匹配。
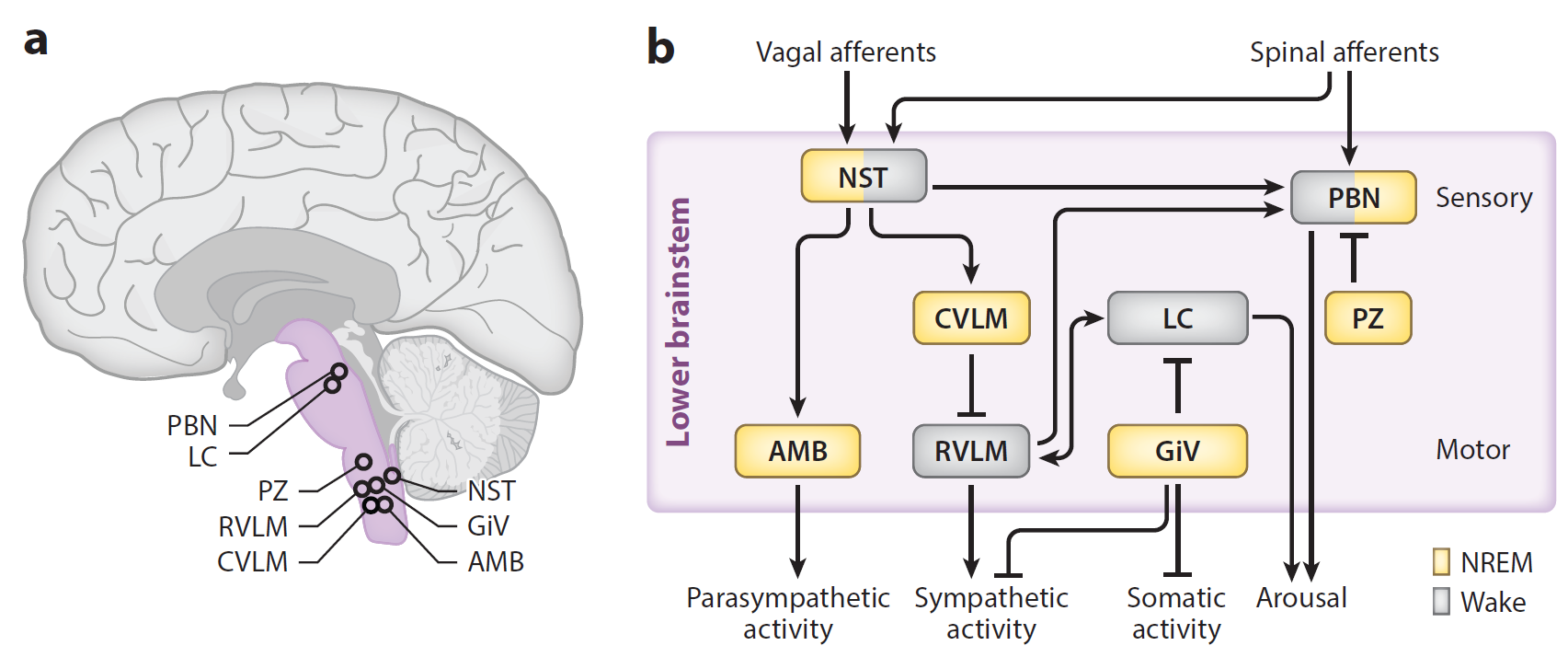
图3. 参与协调外周生理信号与睡眠-觉醒调控的下位脑干核团。
总体而言,睡眠不仅仅是大脑活动状态的改变,更是机体生理状态与大脑状态协同调控共同作用的结果。下位脑干相关核团在这一过程中发挥着重要作用(图3):孤束核作为内脏感觉信息进入中枢并转化为睡眠驱动的主要门户;臂旁核在处理威胁相关输入和促进觉醒方面具有关键作用;腹外侧延髓和蓝斑核中的儿茶酚胺能神经元参与应激相关觉醒调控,并与疑核胆碱能神经元、以及分布于多个延髓区域的GABA能神经元则协同调控睡眠-觉醒状态、躯体运动和自主神经活动。这些核团共同构成了连接身体内部状态与大脑状态调控的关键环路。该框架的提出,不仅为理解睡眠的生理功能提供了新的理论基础,也为研究睡眠障碍及其与代谢、免疫和心血管疾病之间的关系开辟了新的方向。
未来,随着技术发展和研究深入,有望系统阐明不同输入如何塑造脑干不同类型神经元活动,并调控睡眠-觉醒状态,从而更加深入地解析不同脑干核团在睡眠调控中的分工与协作机制,揭示身体-大脑整合在睡眠生理和相关疾病中的重要意义。
题目:Body-Brain Integration: The Lower Brainstem in Sleep-Wake Regulation
作者:Yuanyuan Yao, Yang Dan
单位:Institute of Neuromodulation and Cognition (INC), Shenzhen Medical Academy of Research and Translation (SMART)
期刊:Annual Review of Neuroscience
上线时间:2026年4月20日(Review in Advance)
*丹扬团队(snc@smart.org.cn)正在招聘博士后,姚园园团队(yyyao@smart.org.cn)正在招聘博士后、科研助理和毕设访问学生,期待大家的加入。